-

- ▲ ⓒ연합뉴스
국내 신약개발 바이오벤처들은 '리보세라닙 쇼크'로 높은 글로벌 임상 3상의 벽을 체감하면서도 이번 일을 성장통으로 삼겠다는 의지를 다지고 있다.
2일 업계에 따르면, 에이치엘비의 표적항암제 '리보세라닙'의 글로벌 임상 3상 결과가 사실상 실패인 것으로 드러나면서 신약 개발 바이오기업 전반에 대한 불신이 퍼지고 있다.
◆ '에이치엘비 쇼크'에 동반하락… 신약개발 바이오벤처들 '발동동'
지난 2일 진양곤 에이치엘비 회장은 "리보세라닙 임상 3상은 실패가 아닌 '임상 지연'"이라고 강조했으나, 시장에서는 비관적으로 받아들이고 있다. 이번 탑라인 결과에서 리보세라닙의 전체생존기간(OS)이 5.8개월 정도인 걸로 파악됐기 때문이다.
진홍국 한국투자증권 연구원은 "이는 이미 중국에서 시판된 리보세라닙의 임상 3상 OS(6.4개월)보다 낮은 수치"라며 "현재 위암 2차 치료제는 사이람자와 파클리탁셀 병용이며 OS는 9.6개월이기 때문에 리보세라닙이 2차 치료제를 목표로 파클리탁셀과 병용을 하려면 OS가 9.6개월 이상이 돼야 한다"고 지적했다.
이 같은 소식에 에이치엘비와 제약·바이오 주가는 물론, 코스닥 시장까지 뒤흔들렸다.
지난 27일 진 회장의 기업설명회(IR) 발표 이후 에이치엘비 주가가 전일 대비 30% 하락하면서 하한가를 기록한 것은 물론, 메지온(-28.02%), 신라젠(-8.25%), 헬릭스미스(-5.01%)도 큰폭으로 주가가 하락했다. 이날 오후 2시 이전까지만 해도 상승세를 보였던 코스닥 지수도 11.16포인트(1.57%) 떨어진 698.21로 장을 마치면서, 24일 만에 700선 아래로 무너졌다.
이에 올 하반기에 임상 3상 결과 발표를 앞둔 바이오 업체에 대한 우려도 고개를 들었다.
메지온은 단심실증 치료제 '유데나필'의 미국 임상 3상 탑라인 발표가 차일피일 미뤄지면서 시장의 우려를 샀다. 올해 6월 말~7월 초로 예정됐던 탑라인 발표 시점에 7월 말~8월로 한 차례 더 연기된 것이다. 이 때문에 메지온의 주가는 지난달 27일부터 2거래일간 46.38% 급락한 바 있다.
헬릭스미스는 오는 10월 중 당뇨병성신경병증 신약물질 'VM-202'의 미국 임상 3상 결과를 내놓을 예정이다. 헬릭스미스는 에이치엘비 쇼크와 메지온 임상 3상 지연으로 인한 유탄을 맞아 지난달 27일 전일 대비 5.01%(1만 200원) 주가가 하락한 데 이어 28일에는 11.08%(2만 1000원)나 주가가 떨어지는 수모를 겪었다.
지난 4월 '인보사 사태'를 야기했던 코오롱생명과학은 오는 9월 중순 이후 미국 임상 3상 재개를 위한 자료를 제출할 계획이다. 최대한 빨리 자료를 제출하려고 했으나, FDA가 이달 중순부터 내달까지 휴가라는 점을 감안해서다.
이번에 탑라인 결과가 나온 에이치엘비의 리보세라닙의 글로벌 임상 3상의 전체 결과는 오는 9월 열리는 유럽종양학회(ESMO)에서 발표된다.
◆ 새삼 체감한 글로벌 임상 3상의 벽… 신약 개발 성공률은 단 9.6%
에이치엘비 쇼크를 겪으면서 시장에서는 글로벌 임상 3상의 벽을 새삼 체감했다는 분위기다. 그러나 신약 개발 과정에서 고배를 마시는 일은 글로벌 제약사들도 빈번하게 겪는 일이다. 신약 개발 성공률은 10%도 안 된다는 점을 명심해야 한다는 게 업계 관계자들의 지적이다.
미국 바이오산업협회(BIO)가 임상시험 모니터링 서비스인 바이오메드트렉커(Biomedtracker)를 통해 10여 년간(2006~2015년) 9985건의 임상시험 성공률을 분석한 결과에 따르면, 임상 1상부터 최종 신약 허가에 이를 가능성은 9.6%인 것으로 나타났다. -
일반적으로 신약의 임상시험 단계별 성공률은 ▲임상 1상 63.2% ▲임상 2상 30.7% ▲임상 3상 58.1% ▲신약승인신청 85.3%인 것으로 확인됐다.
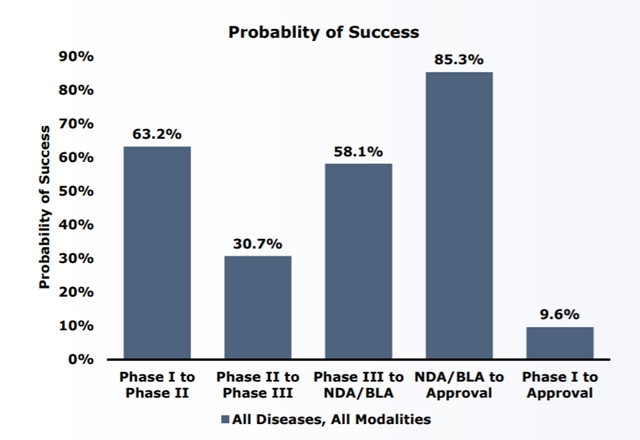
- ▲ 신약의 임상시험 단계별 성공률 ⓒBIO, Biomedtracker, Aplion
항암 신약의 성공률은 ▲임상 1상 62.8% ▲임상 2상 24.6% ▲임상 3상 40.1% ▲신약승인신청 82.4% 등으로 가장 낮은 편이다. 희귀 질환 신약의 경우 ▲임상 1상 76.0% ▲임상 2상 50.6% ▲임상 3상 73.6% ▲신약승인신청 89.2% 등으로 각 임상단계별 성공률이 다소 높아진다.
다만, 업계에서는 이번 일로 인해 신약개발에 열중하는 바이오벤처에 대한 투자가 줄어드는 것을 경계했다. 바이오벤처의 자금 지원 경로가 다양해질 필요가 있다는 제언도 나왔다.
한 업계 관계자는 "신약개발하는 회사들이 임상시험을 하면서 실패를 겪을 수도 있는 것은 당연한 일"이라며 "이 때문에 투심이 악화돼서 자금 수혈이 잘 되지 않으면 신약개발하는 바이오벤처 쪽은 상당히 힘들어질 수도 있다"고 말했다.
업계에서는 이번 일을 계기로 삼아 국내 바이오산업 발전에 더욱 힘쓰겠다는 입장이다.
이승규 한국바이오협회 부회장은 "(국내 제약·바이오사들이) 미국 임상의 문을 두드리기 시작한 것도 상당히 발전한 것"이라며 "지금 이 과정은 지극히 정상적이고 K-바이오가 튼튼해지기 위한 성장통"이라고 진단했다. 이어 그는 "임상 실패에 대해 너무 일희일비하기보다는 바이오산업이 건전화돼는 과정에 주목해달라"고 당부했다.
높은 美 임상 3상의 벽… "에이치엘비 쇼크 'K-바이오 성장통' 삼겠다"
- 김새미 기자
입력 2019-07-02 15:18수정 2019-07-02 15:25
공유하기
기사 공유하기
'에이치엘비 쇼크'에 동반하락… 신약개발 바이오벤처들 '발동동'새삼 체감한 글로벌 임상 3상의 벽… 신약 개발 성공률은 단 9.6%
김새미 기자







