-
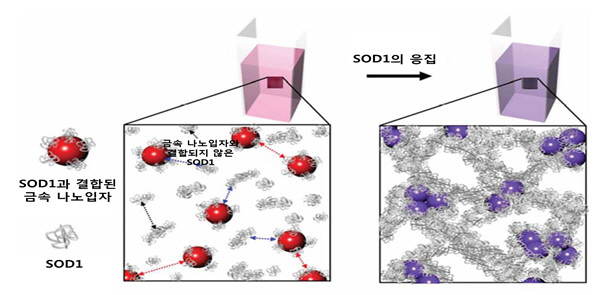
- ▲ SOD1 응집체의 구조 변화에 따른 나노입자 용액의 색상 변화ⓒ 교과부 제공
치매와 루게릭병, 알츠하이머병의 공통점은? 정답은 '신경퇴행성' 질환이다. 이들 질병은 신경세포 안과 밖에 존재하는 특정한 단백질의 이상 응집에 따라 발생하는 것으로 알려져 있다.
따라서 이들 질병의 진단 및 치료에 있어서 가장 중요한 것은 그 원인이 되는 단백질 변화를 신속하고 정확하게 측정하는 것이다.
-

- ▲ 이종협 서울대 화학생물공학부 교수ⓒ 교과부 제공
-

- ▲ 강태욱 서강대 화공생명공학과 교수ⓒ 교과부 제공
국내 연구진이 고가의 실험장비 도움 없이도 질병의 원인이 되는 단백질 변화를 빠르고 정확하게 측정하는 신기술 개발에 성공했다.
서울대 이종협 교수팀(화학생물공학부)과 서강대 강태욱 교수팀(화공생명공학과)은 금 나노입자를 이용, 질병의 원인이 되는 단백질 변화를 측정하는 새로운 기술을 개발했다.
특히 이번 연구는 그 중요성을 인정받아 화학분야의 권위 있는 학술지인 ‘케미컬 커뮤니케이션즈(Chemical Communications)’ 2월호에 게재되면서 동시에 표지논문으로 선정됐다.
일반적으로 치매, 루게릭병, 알츠하이머병과 같은 신경퇴행성 질환은 신경세포 내외에 존재하는 특정한 단백질의 이상 응집에 따라 발생한다.
단백질의 이상 응집현상을 관찰하고 이해하는 것은 이들 질병의 진단이나 치료제 개발의 핵심 요소다.
그러나 고가의 복잡한 실험장비를 사용하지 않고서는 단백질 변화 양상을 생체조건에서 실시간으로 관찰하는 것이 불가능했다.
공동연구팀은 금나노 입자가 20nm이하에서는 붉은색을 띠다가 나노입자 사이의 거리가 가까워지면 나노입자의 상호작용에 따라 점점 짙은 보라색을 띠는 성질에 착안, 이같은 문제점을 해결키 위한 연구를 시작했다.
우선 공동연구팀은 금나노 입자에 SOD1 단백질을 고정시켜 센서를 제작한 후 SOD1 단백질 응집에 따른 금나노 입자의 색 변화를 관찰했다.
SOD는 ‘슈퍼 옥사이드 디스뮤타제(Superoxide dismutase)’의 약자로 인체 내 활성산소(독성산소)를 산소와 과산화수소로 바꿔 세포를 보호하는 '항산화제'다. ‘루게릭병(ALS)’은 바로 SOD의 변화가 원인인 것으로 알려져 있다.
연구팀은 SOD1 단백질이 응집체를 만들면서 금 나노 입자도 같이 응집, 수용액의 색이 붉은색에서 점점 짙은 보라색으로 변해가는 것을 육안으로 관찰 할 수 있었다.
이종협 교수는 “이번 연구를 통해 단백질 응집체의 변화 양상을 관찰할 수 있는 기반을 제공, 루게릭병 등의 발병원인 파악과 조기진단 가능성을 보여줬다”고 연구 의의를 설명했다.
한편 이번 연구는 교과부 ‘21세기프론티어 나노소재사업단’과 ‘WCU육성사업’의 지원을 받아 이뤄졌다.
-

- ▲ 연구논문이 실린 ‘케미컬 커뮤니케이션즈(Chemical Communications)’ 2월호 표지ⓒ 교과부 제공
화학분야 세계적 권위지 표지 논문 선정
국내연구진, 루게릭 등 난치병 조기진단 신기술 개발
- 관리자
입력 2012-02-10 13:25수정 2012-02-10 16:19
공유하기
기사 공유하기
서울대 이종협, 서강대 강태욱 교수팀 공동연구금나노 입자 이용, 인체단백질 구조변화 측정 성공루게릭병 등 단백질 이상 질환 조기진단 가능성 보여줘
관리자







