이달 중 美 FDA에도 임상 1상 IND 신청 계획GLP-1/GIP/글루카곤 삼중 작용제
-
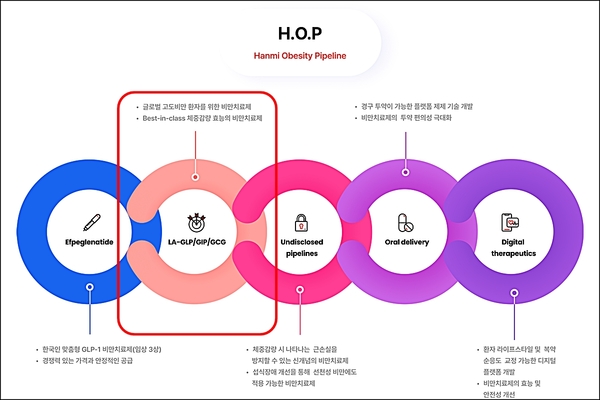
- ▲ ⓒ한미약품
한미약품이 지난 2월29일 식품의약품안전처에 비만치료제 후보물질 ‘HM15275’의 임상 1상 시험계획(IND)을 제출했다고 8일 밝혔다. 이달 중 미국 식품의약국(FDA)에도 IND를 신청할 계획이다.HM15275는 글루카곤 유사 펩타이드(GLP-1)와 위 억제 펩타이드(GIP), 글루카곤(GCG) 등 수용체 3종을 동시에 작용하도록 최적화한 비만치료제 후보물질이다.GLP-1 수용체 작용제는 포만감을 증가시켜 체중을 감소시키고 인슐린 분비와 감수성을 개선해 혈당 조절을 원활하게 한다. GIP는 GLP-1 수용체 작용제의 약리학적 이점을 높일 뿐만 아니라 메스꺼움과 구토, 설사 등의 위장관 부작용을 완화할 수 있다. 글루카곤은 포만감 조절 및 에너지 소비 및 지질 대사 조절에 관여한다.한미약품은 비만뿐만 아니라 제2형 당뇨병, 심혈관 질환 등 대사질환 치료제 가능성도 모색 중이다.한미약품은 HM15275가 우수한 체중감량 효능은 물론, 심혈관 및 신장 질환에 대한 개선 효과를 나타내는 ‘차세대 비만치료제’가 될 것으로 기대하고 있다.비임상 연구에서 HM15275는 근 손실을 최소화하면서도 수술적 요법과 비슷한 수준의 체중감량 효과가 나타났다. 다양한 대사질환 모델에서도 기존 비만치료제보다 우수한 치료효과를 확인했다.한미약품은 임주현 한미사이언스 전략기획실장의 리더십 아래 비만치료, 관리, 예방 등 전주기적 치료 방법을 모색하는 ‘H.O.P 프로젝트’를 추진 중이다.H.O.P 프로젝트에는 HM15275 외에도 현재 임상 3상 시험 중인 ‘에페글레나타이드’, GLP-1 제제 사용시 나타날 수 있는 근육량 손실을 방지해 주고 요요 현상을 억제해 주는 바이오신약, 섭식장애 개선제, 경구용 비만치료제, 비만 예방과 관리에 적용할 수 있는 디지털치료제 등이 포함됐다.한미약품 관계자는 “기존 치료제의 한계를 극복하고 효과를 혁신적으로 높이는 차세대 비만 치료제 개발을 완수할 수 있도록 최선을 다하겠다”고 말했다.한편, 한미약품은 오는 6월 미국에서 열리는 2024 미국 당뇨병학회(ADA)에서 HM15275 연구결과를 발표할 예정이다.







