-

- ▲ 신라젠 CI ⓒ신라젠
신라젠이 항암 바이러스 '펙사벡'의 간암 대상 임상 3상이 중단되면서 존폐기로에 섰다. 신라젠은 간암 외 다수 암종을 대상으로 병용요법·술전요법(암세포 크기 축소) 임상을 진행하겠다는 계획을 밝혔지만, 회생 여부는 불투명하다.
신라젠은 4일 서울 여의도에서 열린 무용성 평가 결과를 보충 설명하기 위한 긴급간담회를 개최했다.
앞서 신라젠은 지난 2일 미국 샌프란시스코의 독립적인 데이터 모니터링 위원회(Independent Data Monitoring Commitee, 이하 DMC)가 항암 바이러스 '펙사벡'의 간암 대상 임상 3상 시험(PHOCUS) 중단을 권고했다고 밝혔다. 무용성 평가에서 펙사벡의 유효성이 입증되지 않아 사실상 펙사벡이 신약으로서 가치가 없는 것으로 판명됐다.
신라젠 측은 "간암 1차 치료제로 펙사벡과 표적 치료제인 '넥사바'와의 순차 투여가 넥사바 단독 대비 생존기간의 향상을 가져오지는 못했다"며 "이는 펙사벡 투여 후 넥사바를 투여하는 것이 간암 환자에서는 효과적이지 못했다는 것을 암시한다"고 인정했다.
그러면서도 "하지만 분당차병원에서 펙사벡 투여 후 면역관문억제제인 '옵디보'를 투여한 결과 완전 반응을 보인 증례가 있어 간암에서도 펙사벡이 표적치료제보다는 면역관문억제제와의 병용 치료가 더욱 효과적임을 알 수 있다"며 "신라젠에서는 여러 암종 대상으로 다양한 면역관문억제제와 병용요법 임상시험을 진행 중이거나 진행할 예정"이라고 강조했다.
앞으로 신라젠은 다수의 암종을 대상으로 병용요법과 술전요법 임상에 집중할 계획이다. 간암의 결과와는 무관하게 타 적응증 병용임상의 효능 데이터가 우수할 수 있다는 기대감에서다. -
신라젠이 진행 중인 펙사벡 병용 임상시험 중 간암 다음으로 가장 앞선 단계에 진입한 암종은 신장암이다.
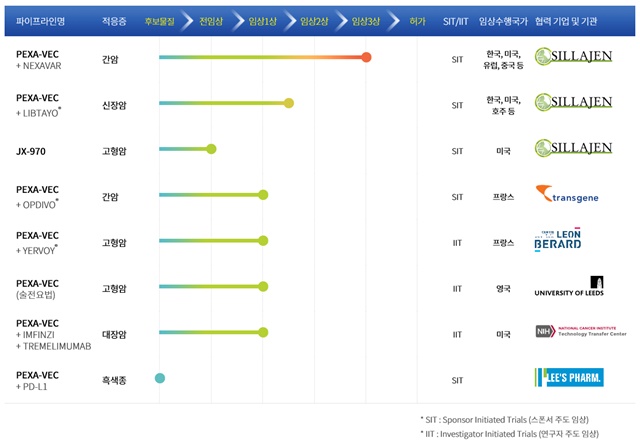
- ▲ 신라젠의 파이프라인 현황 ⓒ신라젠
신라젠은 표적치료제에 반응하지 않는 신장암 환자 대상으로 미국 리제네론사의 면역관문억제제 '리브타요'와 펙사벡 병용 투여 임상시험을 진행 중이다.
5명의 환자를 대상으로 한 용량 결정 임상시험에서 1명의 완전반응, 1명의 부분반응, 1명의 안전병변, 2명의 진행 결과를 확인했다. 현재 펙사벡과 리브타요 병용요법에 대한 환자군 11명을 모집 완료해 주기적인 CT 촬영을 통해 경과 관찰 중이다.
또한, 신라젠은 미국국립암연구소(NCI)에서 면역관문억제제 불응성 암종인 대장암을 대상으로 아스트라제네카사의 '임핀지'와 펙사벡 병용요법 임상을 진행하고 있다.
등록된 환자 중 1명에서 통증의 감소와 대장암 암수치의 정상, CT 촬영 결과 부분반응을 보였다. 신라젠은 해당 치료 효과에 대한 결과를 내년 1월에 열리는 미국임상종양학회 위장관종양 심포지엄(GI ASCO)에 초록 접수할 예정이다.
신라젠은 유방암 환자 중 간에 전이된 환자를 대상으로 머크사의 '키트루다'와 펙사벡을 병용하는 임상시험도 진행할 계획이다. 현재 임상 프로토콜과 임상진행 병원 선정은 완료했으며, 내년 1분기 내 첫 환자 등록을 계획하고 있다.
소화기 암종(대장암, 췌장암, 담도암, 위암), 기타 암종(폐암, 흑색종 등) 또는 기존의 면역관문억제제 불응성 간 전이가 있는 환자를 대상으로 BMS사의 '옵디보'와 펙사벡 종양내 투여를 병용하는 임상시험도 곧 개시할 방침이다.
신라젠 측은 "호주의 한 대학병원에서 전립선 암 수술 전 펙사벡을 종양 투여·정맥 투여하는 임상시험을 준비하고 있다며 "국내 대학병원에서는 두경부암과 부인암 대상으로 술전요법을 계획하고 있다"고 강조했다.
다만, 신라젠의 이 같은 계획이 성공할 수 있을지는 미지수다. 이미 한 차례 펙사벡의 글로벌 임상 3상이 실패했기 때문에 시장의 신뢰를 회복하긴 어려울 것으로 보인다. 넥사바를 지외한 병용요법은 임상 1~2상에 머물러 있기 때문에 임상 3상에 진입하기까지 많은 시간이 걸린다는 점도 걸림돌이다.
업계 관계자는 "이미 글로벌 임상 3상이 실패한 펙사벡이라는 물질 하나로 계속 임상시험을 한다는 것은 방법이 없다는 뜻으로도 비친다"며 "아무래도 신라젠이 회생하기는 어려울 것 같다"고 말했다.
[신라젠 쇼크] 존폐기로 속에서 '펙사벡 임상 실패' 이후 계획은?
- 김새미 기자
입력 2019-08-04 13:07수정 2019-08-04 15:05
공유하기
기사 공유하기
신라젠, 4일 서울 여의도서 무용성 평가 결과 보충 설명 긴급간담회 개최"펙사벡, 간암 1차 치료제로서 효과 없었지만 다른 암종 대상 병용임상 진행""펙사벡, 표적치료제보다는 면연관문억제제 병용요법이 효과적일 수 있어"
관련기사
김새미 기자







