핵인의 구조·물성 변형과 비정상적 단백질 응집 촉진 관찰생화학·분자생물학 분야 국제학술지 'Redox Biology'에 게재
-

- ▲ 권영대 교수 연구팀.ⓒ성균관대
성균관대학교는 의학과 권영대 교수 연구팀이 노화가 진행될 때 세포 내 핵인의 분자 확산성이 감소하는 등의 특성 변형이 수반되는 것을 확인했다고 9일 밝혔다. 노화 조절 인자 발굴이나 퇴행성 질환에 대한 신규 표적 치료 가능성에 관심이 쏠린다.노화는 그동안 거스를 수 없는 생명 현상으로 여겨졌으나 세포 노화에 관한 연구가 쌓이면서 인류가 극복할 대상으로 인식이 바뀌고 있다. 세포 노화는 유전체 불안정성, 활성산소종, 만성적 염증 등으로 인해 세포의 증식 능력이 감퇴한 상황이다. 알츠하이머병, 관절염, 망막 변성, 근감소증 등의 퇴행성 노인질환과 밀접한 관계가 있다고 알려졌다.핵인(Nucleolus)은 세포 내 단백질 생산을 담당하는 리보솜이 조립되는 비막성 세포소기관이다. 핵인의 물질적 특성은 다른 주변의 핵질과 분리된 채 독자적인 액체상 방울 형태로 존재하며, 이는 기름이 물에 섞이지 않고 액체 방울로 떠 있는 것과 비슷하다. 핵인처럼 생체막을 활용하지 않은 채 물리적 성질에 의해 주변과 분리된 세포 내 구조체를 생체분자 응축상(Biomolecular condensate)라고 한다. 세포생물학 분야에서 물질적 특성 분석이라는 새 관점으로 생체분자 응축상을 연구하는 시도가 활발하게 이뤄지고 있으나 노화 현상을 이해하는 데 이런 연구 전략이 적용된 적은 없었다. -
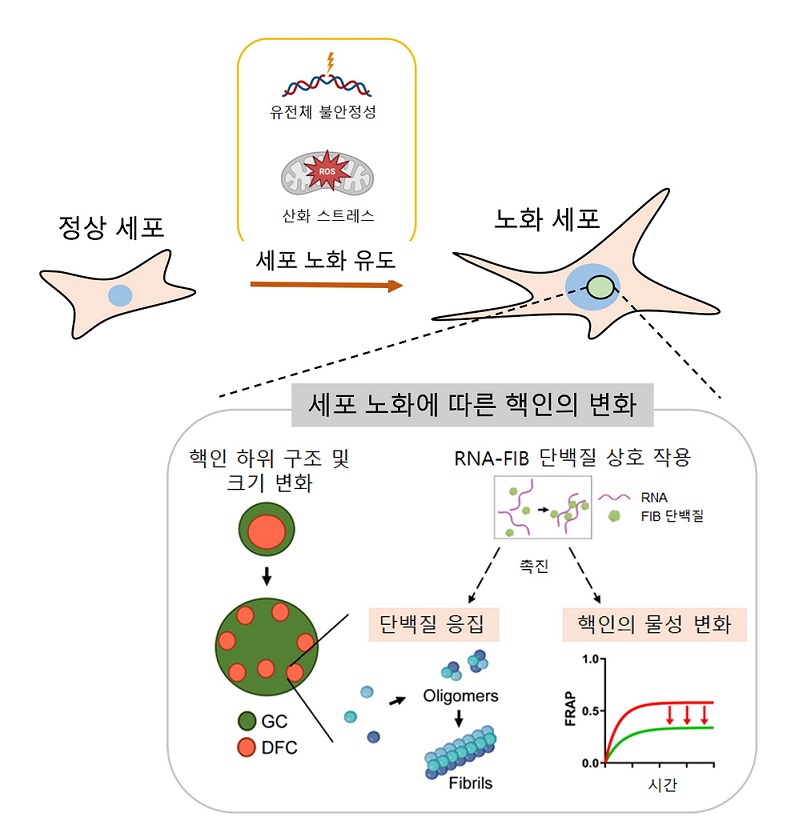
- ▲ 세포 노화에 의한 핵인 차원 신규 표현형 규명.ⓒ성균관대
권 교수 연구팀은 세포 분열이 정지된 노화세포에서 핵인이 해체-재구성 과정을 거치지 않고 오랫동안 유지된다는 점에 착안해 핵인의 형태와 유동성 등의 특성이 변형될 것이라는 가설을 세웠다. 연구팀은 이를 확인하기 위해 DNA 손상, 후성유전적 변화 등 유전체 불안정성이 증대되거나 활성산소종이 처리돼 노화가 유도된 세포 모델을 활용했다. 확인 결과 노화세포의 경우 핵인의 하위 구조 중 리보솜 RNA의 안정화·성숙화가 이뤄지는 밀집 섬유 중심(DFC) 영역의 형태가 정상 세포와 큰 차이가 있는 것으로 나타났다.또한 DFC 영역 내에서 분자 확산성이 감소하는 동시에 분자 간 밀집도는 증가하는 등 물질적 특성이 변형됐다. 퇴행성 질환에서 흔히 발견되는 단백질 응집이 형성되는 과정에서 나타나는 다량체와 섬유소 등의 병리적 단백질 구조들이 노화 세포의 DFC 영역에서 증가하는 게 관찰됐다.연구팀은 앞으로 핵인 내 노화 조절 인자 발굴 등 후속 연구를 진행할 계획이다. 권 교수는 "세놀리틱 혹은 세노몰픽 전략 등을 통한 항노화 연구·개발이 급증하는 상황에서 약리 효능을 독창적으로 평가할 수 있는 지표를 개발했다"며 "퇴행성 질환들에서 발견되는 단백질 응집 현상을 기반으로 한 질환 치료 신규 표적을 탐색해 나갈 것"이라고 말했다.이번 연구 결과는 생화학·분자생물학 분야 국제학술지 'Redox Biology'에 지난달 25일 온라인 게재됐다. 권 교수가 교신저자, 조민정 학생이 제1저자로 참여했다. 이번 연구는 한국연구재단의 우수신진연구사업, 한국과학기술연구원(KIST)-성균관대(SKKU) 융합연구사업의 지원으로 이뤄졌다. -

- ▲ 성균관대학교 전경. 우측 하단은 유지범 총장.ⓒ성균관대







