소아 백혈병 대상 연구 진행… 政 “치료기획 제공 등 성과 기대”
-
- ▲ ⓒ보건복지부
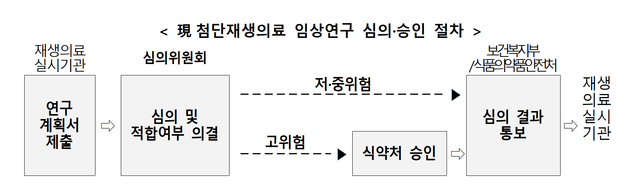
‘키메라항원수용체 T세포(CAR-T)’를 활용한 소아 백혈병 치료가 국내 첫 고위험 첨단재생의료 임상연구로 승인됐다.보건복지부, 식품의약품안전처는 8일 강형진 서울대병원 소아청소년과 교수가 신청한 이 같은 임상연구 계획을 승인했다고 밝혔다.이번 건은 ‘사람의 생명 및 건강에 미치는 영향이 불확실하거나 그 위험도가 큰 임상연구’로 분류된다. 이전의 치료와는 다른 획기적인 방법으로 희귀난치질환자들의 치료 등이 가능하나 위험도가 높은 만큼 안전성과 유효성에 대한 세밀한 심사가 진행됐다.임상연구의 주요 목표는 CAR-T를 사용한 소아청소년 급성 림프모구백혈병 환자의 치료에 성과를 내는 것이다. 그간 항암화학요법 등 치료가 진행됐으나 재발성·불응성 환자의 경우 치료에 한계가 있었다.김영학 복지부 재생의료정책과장은 “이번 고위험 임상연구 1호 승인 이후 다양한 희귀난치질환에 대한 임상연구를 통해 희귀난치질환자들의 치료 기회를 제공하고, 추후 많은 환자들에게 제공될 수 있는 치료제가 개발되기를 기대한다”고 밝혔다.이어 “임상연구계획 심의 등 법령에서 요구되는 안전성, 유효성 등을 철저히 검증하면서 임상연구비 지원사업·범부처 재생의료기술개발사업 등 관련 사업을 통해 재생의료 분야의 진흥에 최선을 다하겠다”고 덧붙였다.







