1차 유효성 평가지표 '12주 시점 EASI50' 통계적 유의성 확보 실패16주차 이후 장기 효과 확인에 고무적인 반응글로벌 빅파마에 기술수출 모색내년 2월 첨생법 시행 맞춘 상업화도 추진다만 국내 품목허가 허가 가능성은 크지 않을 듯
-

- ▲ 나종천 강스템바이오텍 대표가 이날 서울 여의도 전경련회관에서 아토피 피부염 줄기세포 치료제 후보물질 '퓨어스템-에이디주'의 임상 3상 시험 결과 발표 기자간담회에서 발언하고 향후 전략을 소개하고 있다.ⓒ최영찬 기자
"퓨어스템-에이디주 임상 3상 시험 1차 유효성 평가지표는 충족 못했지만 임상적 의미를 분석한 뒤 식품의약품안전처에 품목허가를 신청하고 국내외 제약사를 대상으로 기술수출을 추진하겠다."나종천 강스템바이오텍 대표이사가 5일 서울 여의도 전경련회관에서 아토피 피부염 줄기세포 치료제 후보물질 '퓨어스템-에이디주'의 두 번째 임상 3상 시험 결과 발표 기자간담회를 갖고 이렇게 말했다.강스템바이오텍은 전날 퓨어스템-에이디주 임상 3상 시험 톱라인 결과를 수령했는데 1차 유효성 평가지표로 삼은 베이스라인 대비 12주 시점 EASI50(습진중증도평가지수 50% 이상 감소) 지표가 통계적 유의성을 확보하지 못했다고 밝혔지만 장기간 효과에서 가능성을 봤다고 판단해서다.배요한 강스템바이오텍 임상개발본부장은 12주차 EASI50과 EASI75 지표에서는 통계적 유의성이 나타나지 않았지만 16주차, 24주차에서는 통계적 유의성을 확보했다고 설명했다.퓨어스템-에이디주의 EASI50 달성률은 16주차 49.04%에서 24주차 58.06%로, EASI75 달성률은 같은 기간 19.11%에서 30.32%로 상승곡선을 그렸다는 것이다.여기에 퓨어스템-에이디주 투여 1년이 지난 뒤 EASI50 달성률은 72.2%, EASI75(습진중증도평가지수 75% 이상 감소) 달성률은 54.1%로 집계됐으며 2년이 지난 뒤 EASI50 달성률은 67.4%, EASI75 달성률은 46.5%로 분석됐다고 했다.나 대표는 세계적으로 아토피 치료제에 대한 니즈가 높은 상황에서 장기효과가 나타난 퓨어스템-에이디주에 대해 글로벌 빅파마들이 높은 관심을 보이고 있어 물밑 작업이 활발히 이뤄지고 있다고 설명했다.이계종 강스템바이오텍 CFO(최고재무책임자) 상무는 "미국에서 1곳, 중국 2곳, 유럽 1곳의 빅파마와 각각의 해당 지역에 대해 퓨어스템-에이디주를 기술수출하는 것을 논의하고 있다"고 귀띔했다.강스템바이오텍은 내년 2월 개정된 '첨단재생의료 및 첨단바이오의약품법(첨생법)' 시행에 맞춰 퓨어스템-에이디주의 상업화도 추진할 계획이다.첨단재생의료의 임상연구 대상 범위가 '모든 사람'으로 확대됐고 기업들이 환자에 비용 청구도 할 수 있게 돼 사실상 첨단재생의료 사업이 가능해졌기 때문이다. 여기에 국내보다 재생의료치료 시장이 큰 일본에 올해 안에 퓨어스템-에이디주 투약을 목표로 관련 절차도 밟고 있다고도 했다.다만 퓨어스템-에이디주의 국내 품목허가 획득 가능성은 높지 않다는 게 업계의 중론이다.퓨어스템-에이디주 투여군의 12주차 EASI50 달성률은 34.18%인 데 반해 위약 투여군은 29.79%로 나타나 통계적 유의성을 확보하지 못했다.국내 허가받은 세포치료제 모두 1차 유효성 평가지표를 충족했다는 점에서 1차 유효성 평가지표를 충족하지 못한 퓨어스템-에이디주에 대한 식약처 허가 가능성은 크지 않다는 것이다.여기에 지난해 4월 네이처셀의 관계사 알바이오가 퇴행성관절염 치료제 후보물질 '조인트스템'에 대해 통계적 유의성을 확보하고도 '임상적 유의성'을 충족하지 못했다는 이유로 품목허가 신청이 거절되는 등 줄기세포치료제 품목허가 기준이 높은 상황이다.이 때문에 오히려 1차 유효성 평가지표를 16주차 이후 EASI50 점수로 바꿔서 임상시험을 다시 해야 하는 게 아니냐는 시선도 나온다.지난 5월 CRO(임상수행기관) 자회사 크로엔 지분 약 50%를 HLB바이오스텝에 매각해 재무 이슈 때문에 나 대표는 이러한 점을 의식한 듯 "글로벌 빅파마뿐만 아니라 국내 제약사에도 기술수출하는 것을 고려하고 있다"고 말하기도 했다.강스템바이오텍은 2018년 4월부터 2019년 10월까지 첫 번째로 진행했던 퓨어스템-에이디주 임상 3상 시험에서도 1차 유효성 평가지표로 삼았던 EASI50에서 통계적 유의성을 확보하지 못한 바 있다.첫 번째 임상 3상 시험 실패 이후 강스템바이오텍은 임상시험용 의약품을 동결보관하는 플랫폼 기술 '셀럽'을 적용하는 등 임상시험 디자인을 대폭 손질했다.제조 후 24시간이 지나면 세포 활성도가 80% 아래로 떨어지고 유효기간도 48시간에 불과했지만 셀럽을 적용해 유효기간을 최대 3년까지 늘리고 투약 직전 의약품을 해동해 높은 세포 활성도를 유지하는 노력을 기울였지만 결국 두 번째 임상 3상 시험에서도 1차 유효성 평가지표 확보에 실패했다.이 때문에 강스템바이오텍은 2025년 2분기 퓨어스템-에이디주의 품목허가를 획득한 뒤 연 매출 2000억원 이상을 올리는 것을 목표로 세웠는데 이 구상에 차질이 빚어질 공산은 커졌다.이날 간담회에 참석한 주주들은 '재무 이슈를 해결하기 위해 또 유상증자를 하는 게 아니냐' '주가가 하한가로 직행했는데 걱정이다' '기술수출 가능성은 얼마나 되냐' 등의 질문을 하기도 했다.나 대표는 "향후 기술수출 등을 통해 자금을 확보할 여지가 충분하다"면서 "현 시점에서 유증 계획은 없다"고 답했다. -
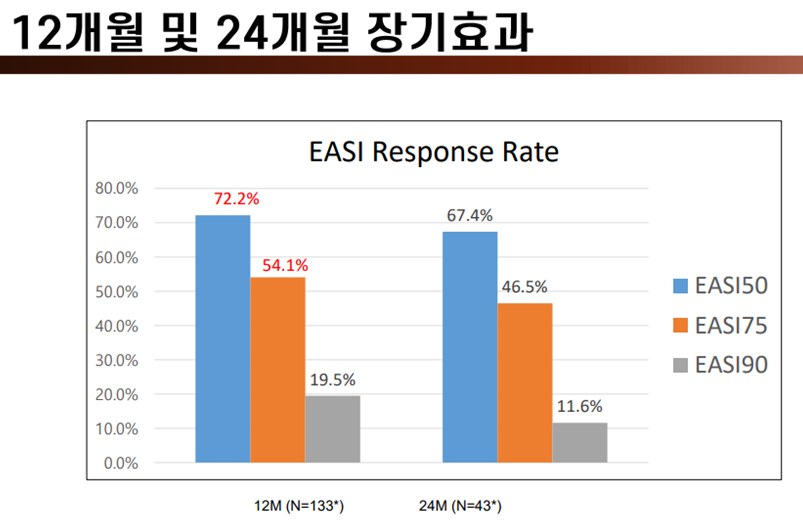
- ▲ ⓒ강스템바이오텍







