광 절단성 단백질 함유 엑소좀을 이용해 타깃 세포 내부로 효과적 전달치료 단백체 전달과 인지능력 개선 등 치료 효과 확인
-

- ▲ 성균관대 약학과 조동규 교수와 한지훈 박사.ⓒ성균관대
성균관대학교는 약학대학 조동규 교수 연구팀이 빛을 이용한 엑소좀 기반 세포 내 치료 단백질 전달 기술을 개발했다고 13일 밝혔다. 조 교수와 ㈜엑소스템텍이 공동 진행한 이번 연구는 엑소좀을 통한 CRISPR 등 치료 단백체를 몸 안에 효과적으로 전달함으로써 알츠하이머 치매 등의 질환 치료에 적용할 수 있을 것으로 기대된다.현재 임상적으로 사용되는 단백질 치료제(단일클론항체, 사이토카인, 호르몬)는 모두 세포 외부에서 작용한다. 하지만 대다수 질병은 세포 내부에 특정 단백질·유전자의 돌연변이 혹은 이들의 기능 장애로 인해 발병한다. 질병을 효과적으로 치료하려면 치료적 단백질을 세포 내부로 전달하는 기술이 필요하다.공동 연구팀은 목적 단백질의 세포 내 전달 매개체로 엑소좀을 이용했다. 연구팀은 광 절단성 단백질인 mMaple3를 목적 단백질과 엑소좀 마커 사이에 융합시켰다. '목적 단백질-mMaple3-엑소좀 마커'로 이뤄진 융합단백질을 엑소좀 생성 세포에 과발현시켜 엑소좀을 추출한 뒤 405-㎚의 빛을 쬐어 mMaple3을 절단시켜 목적 단백질을 엑소좀 마커로부터 분리했다. 연구팀은 빛을 쬔 엑소좀이 목적 단백질을 효과적으로 타깃 세포 내부로 전달한다는 사실을 확인했다. -
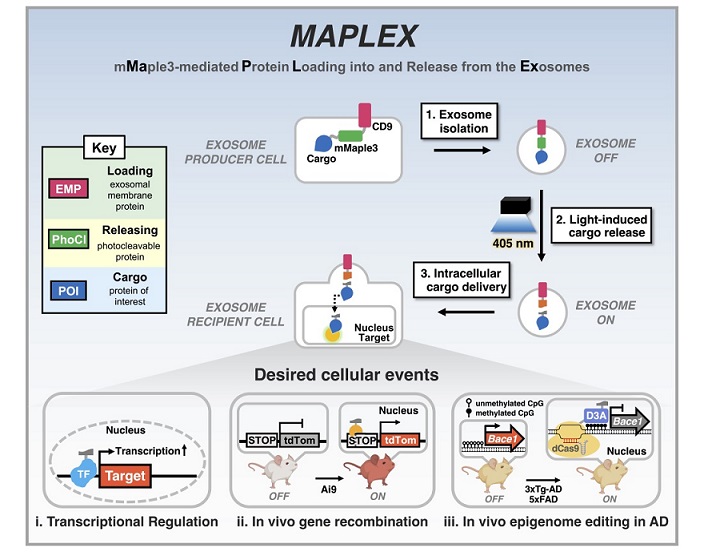
- ▲ 조동규 교수가 개발한 MAPLEX 시스템과 이의 응용.ⓒ성균관대
더 나아가 연구팀은 이 MAPLEX 시스템을 이용해 CRISPR/Cas 기반 후성유전학 편집기를 알츠하이머 모델 마우스인 3xTg-AD와 5xFAD의 뇌에 효과적으로 전달함으로써, 아밀로이드 생산 효소인 Bace1의 발현을 감소시키고 인지기능 개선 등의 치료 효과를 확인했다.조 교수는 "바이러스 사용 없이 다양한 치료 단백질을 세포 내부로 효과적으로 전달할 수 있는 새로운 전달체계를 개발한 것"이라며 "이 시스템을 이용해 CRISPR 기반 유전자 교정과 다양한 치료 단백질의 전달이 가능할 것이다. 다양한 질환 치료제 개발이 가능할 것"이라고 말했다.이번 연구 논문(Engineered exosomes with a photoinducible protein delivery system enable CRISPR/Cas-based epigenome editing in Alzheimer’s disease)은 의학 분야의 세계적 학술지 'Science Translational Medicine'에 지난 7일 발표됐다. 제1 저자로는 성균관대 약학대 한지훈 박사가 참여했다. 이번 연구는 한국연구재단의 중견연구자지원사업과 선도연구센터(MRC) 등의 지원을 통해 이뤄졌다. -

- ▲ 성균관대학교 전경. 우측 하단은 유지범 총장.ⓒ성균관대







