DNA-셀룰로스 나노복합체로 정교한 암세포 표적 가능암 조직의 환경에서만 약물 방출 … 효율적 항암 치료법 제시고분자 분야 세계적 학술지 '카보하이드레이트 폴리머'에 실려
-

- ▲ 왼쪽부터 연세대 이유연 석사, 남건욱 박사, 노영훈 교수.ⓒ연세대
연세대학교는 생명공학과 노영훈 교수 연구팀이 첨단 나노소재를 활용해 암세포를 정확하게 표적하고, 암세포 환경에서만 약물을 방출하는 새로운 약물 전달 플랫폼을 개발했다고 4일 밝혔다.이번 연구는 항암 치료의 핵심 과제인 약물의 표적 전달과 부작용 문제를 해결하는 데 중점을 두고 있다. 연구팀은 DNA 나노구조체와 나노셀룰로스를 결합한 하이브리드 나노복합체를 개발했다. 이를 통해 특정 암세포만을 정밀하게 표적하고, 암 조직의 산성 환경에서만 약물을 방출하는 차세대 항암 치료법을 제시했다.암 치료는 약물이 건강한 조직을 훼손하지 않고, 종양 부위로만 정확하게 전달되는 것이 핵심 과제다. 이를 위해 pH(산성도), 효소, 빛, 열 등 다양한 환경 변화에 반응해 특정 세포를 표적하고 약물을 방출하는 3D DNA 나노구조체를 사용해 왔다. 그러나 3D 나노구조체는 부작용을 최소화하는 덴 효과적이지만, 생체 내 불안정성과 낮은 약물 탑재량이 한계로 지적돼 왔다. -
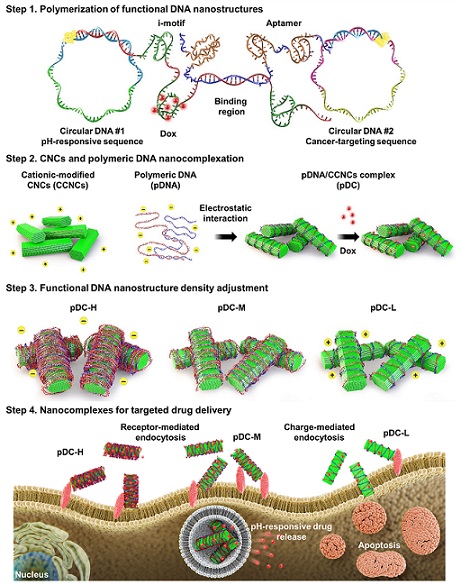
- ▲ 핵산나노공학 기술을 활용하여 고분자화된 기능성 DNA 나노구조체와 표면 개질된 나노셀룰로오스 복합체를 형성하는 과정의 모식도.ⓒ연세대
연구팀은 '회전환복제기법(Rolling Circle Amplification)'로 합성된 고분자형 DNA 나노구조체와 나노셀룰로스를 결합해 생체 내 안정성과 약물 전달 능력을 크게 향상했다.나노셀룰로스는 식물에서 유래한 친환경 소재다. 세포 내 흡수율이 높고 생분해성이 뛰어나 약물 전달체로 적합하다. 연구팀은 나노셀룰로스의 표면을 양전하로 개질해 음전하를 띠는 DNA 나노구조체와 정전기적 결합을 유도함으로써 나노복합체를 합성했다.이 나노복합체는 암세포 표면에 과다 발현된 뉴클레올린 수용체를 표적으로 삼는 압타머(Aptamer)와 암 조직의 pH에 반응해 약물을 방출하는 i-motif 서열로 구성된 고분자 DNA를 포함한다. 연구팀은 다양한 비율로 합성된 나노복합체를 시험해 생체 안정성과 DNA 서열의 기능을 평가했다.실험 결과 생리학적 환경에서 나노복합체의 DNA 함량에 따라 생체 내 안정성, 세포 내 약물 전달 효율, 항암 치료 효과가 크게 달라졌다. 높은 DNA 비율의 전달체는 압타머에 의존해 세포 내로 전달됐고, 약물 방출 효율이 높았으나 안정성이 낮았다. 반면, 낮은 DNA 비율의 복합체는 압타머 기능보다는 전달체의 표면 전하에 주로 의존해 세포 내로 전달됐고, 안정성은 높지만, 약물 방출량이 적었다.이를 토대로 최종 개발된 나노복합체는 암세포를 효과적으로 표적하고, pH 감응성 약물 방출 기능을 탑재해 항암 치료 효과를 최적화했다. 나노셀룰로스의 고유 특성과 DNA의 다기능성을 결합한 이 기술은 암 치료를 위한 혁신적인 나노 융합 전달 플랫폼으로 활용할 수 있다.노 교수는 "이번 연구는 특정 질병 조직 부위에 표적-침투-약물 방출이 쉬운 DNA-셀룰로스 나노복합체를 도입해 부작용이 최소화된 항암 치료제 전달법을 제시하고, 항암 효과를 극대화한 것"이라며 "siRNA, mRNA, DNAzyme 등 다양한 핵산 기반 기능성과 약물을 도입할 수 있어 폭넓은 응용이 가능하다"고 말했다. 이어 "이번 연구에 사용된 핵심 융복합 기법은 DNA 나노구조체 생산 기술과 친환경 나노셀룰로스 공정 기법을 사용하므로 다양한 의료·나노바이오 분야와 대량생산이 가능한 차세대 고부가가치 산업에 적용할 수 있을 것"이라고 덧붙였다.이번 연구 결과는 세계적인 학술지 '카보하이드레이트 폴리머' 9월호에 게재됐다. 노 교수가 교신저자, 이유연 석사·남건욱 박사가 공동 제1저자, 김영민·양경직 박사, 김영목 학생, 오종원 교수가 공저자로 참여했다.이번 연구는 한국연구재단 바이오의료기술개발사업, 기본 연구 등의 지원으로 수행됐다. -

- ▲ 언더우드관.ⓒ연세대







