-
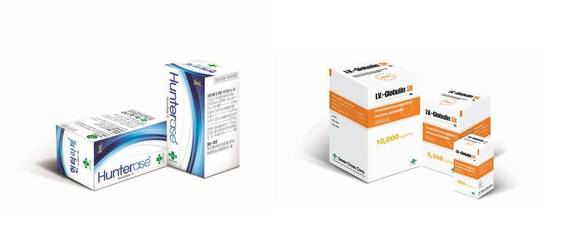
- ▲ 희귀병 헌터증후군 치료제 '헌터라제'(左), 면역결핍 치료제 '아이비글로불린에스엔'(右)ⓒ녹십자
한미약품의 7조5천억원 규모 기술이전 잭팟에 이어 글로벌 신약으로 '제약강국 코리아'를 이끌 국내 제약사들의 신약 개발 움직임이 분주하다.
글로벌 임상을 계획하고 있는 녹십자(회장 허일섭)는 시장 규모가 1조원에 달할 것으로 예상되는 희귀병 헌터증후군 '헌터라제'를 글로벌 시장에 내놓고, 시장의 절반 이상 점유를 목표로 하고 있다. 헌터증후군 치료제 성장률은 연간 11%에 이른다.
이는 특히 다국적제약사의 독무대였던 희귀질환치료 분야에서 주목 받고 있어, 괄목할 만한 성과라는 평가다. 20일 업계 관계자에 따르면 스위스 노바티스 사의 경우 표적항암치료제 '글리벡' 한 알로 5조원이 넘는 매출고를 올렸다며 녹십자의 헌터라제는 전 세계에 제조 가능한 곳이 미국과 녹십자 뿐이므로 기대감이 높다고 전했다.
-

- ▲ 녹십자 화순공장 전경ⓒ녹십자
나아가 녹십자는 주력사업인 혈액분획제제(혈액의 혈장에서 면역이나 지혈 등의 작용을 하는 단백질만을 골라낸 의약품)를 20조원 규모인 북미시장에 공략할 방침이다. 대표적으로 과다 출혈 쇼크를 방지하는 '알부민'과 면역결핍 치료제 '아이비글로불린에스엔', 혈우병 치료제 '그린진 에프'가 있다.
이 가운데 '아이비글로불린에스엔'은 현재 임상3상을 완료해 올해 미국 식품의약국에 품목 허가를 신청할 계획이다. 또한 녹십자는 북미시장 진출에 속도를 내기 위해 지난 해 4월, 캐나다에 혈액분획제제 공장을 건설하고 캐나다 현지법인(GCBT)을 통해 캐나다 관계 기관과 공장 건설 자금지원 및 생산되는 제품을 주 정부가 우선 구매해준다는 내용의 계약을 체결했다. 북미시장에서 녹십자는 연 3000억원 이상의 매출을 예상하고 있다.
'GCBT'는 올 상반기 내로 캐나다 공장 착공에 들어가 2019년까지 완공과 보건성 제품 등록을 완료할 계획이다. 연간 최대 100만 리터 혈장을 처리해 알부민과 면역글로불린 등을 생산할 예정이다. 녹십자 측은 "이번 캐나다 공장 건설이 더 큰 시장인 미국 시장에 안정적으로 진입할 수 있는 계기가 될 것으로 기대한다"는 입장이다.
-

- ▲ 수퍼항생제 시벡스트로ⓒ동아에스티
국내 제약업체 중 가장 많은 국내 신약을 보유하고 있는 동아에스티(대표 김원배)는 지난 달, 당뇨병치료제 '슈가논'의 식약처 허가를 따냈다. 슈가논은 에보글립틴 5mg을 주성분으로 하는 DPP-4(Dipeptidyl peptidase-4) 저해기전의 경구용 혈당강하제이다.
동아에스티는 국내 임상단계부터 활발히 '슈가논'의 해외개발을 추진해 지난 2012년에는 중국 루예 및 인도 알켐 사와, 2014년과 2015년에는 브라질 유로파마 사와 브라질과 중남미 17개국과 계약을 체결했다. 올해는 러시아 게로팜 사와 러시아, 우크라이나, 카자흐스탄에 대한 에보글립틴의 개발과 판매에 관한 라이센싱 아웃 계약을 체결한 바 있다.
동아에스티 박찬일 사장은 "슈가논은 동아에스티가 자체 개발한 5번째 신약으로 스티렌, 자이데나, 모티리톤, 시벡스트로에 이어 동아에스티의 우수한 R&D 기술력을 보여주는 제품이다"며 "국내 허가를 계기로 국내 시장뿐 아니라 해외 시장 진출에 보다 탄력을 받을 수 있을 것으로 기대된다"고 말했다.
자체 개발한 수퍼항생제 타깃 항생제 '시벡스트로'는 지난 해 미국을 시작으로 올초 유럽에서도 허가를 받아 독일, 영국, 덴마크 등에서 판매되고 있다. 또 글로벌 임상 3상 시험을 통해 폐렴에 대한 치료효과를 추가로 검증하고 있어 이 부분에 대한 효능효과가 추가될 전망이다.
세계 최초로 유전성 비만 질환 치료제 개발에 착수하고 있는 종근당은 자프겐 사와 고도비만치료제 'CKD-732'에 대한 라이센싱 아웃 계약을 체결했다. 현재 고도비만은 2상에 있으며, 유전성 비만 질환인 프래더-윌리증후군(PWS)은 3상에 있다.
-
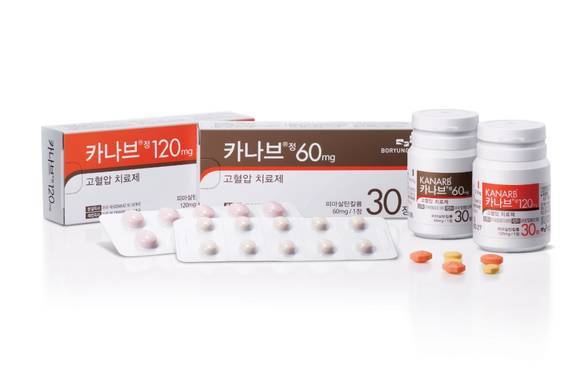
- ▲ 고혈압 신약 카나브ⓒ보령제약
국내 최초 고혈압 신약 '카나브'를 선두로 글로벌 신약 개발에 고삐를 쥐고 있는 보령제약(대표 최태홍)은 ARB(Angiotensin II Receptor Blocker:안지오텐신Ⅱ 수용체 차단제)계열 치료제 카나브에 대한 라이센싱 아웃 계약을 지난 7월과 8월 동남아 13개국과 맺었다.
카나브는 현재 중남미 13개국 중 6개국(멕시코, 에콰도르, 온두라스, 코스타리카, 엘살바도르, 파나마)에서 발매허가를 받았으며, 나머지 중남미 국가들도 2016년까지 발매 허가를 모두 완료할 예정이다.
중남미 13개국 이외에도 2012년 계약한 브라질에서도 이뇨복합제 2상을 성공적으로 마무리한 것은 물론, 2018년 1, 2분기 걸쳐 단일제와 이뇨복합제에 대한 허가를 받을 예정이다. 또한 2013년 계약한 러시아에서도 임상 3상을 성공적으로 마무리하고 현재 결과보고서와 발매 허가 신청을 준비하고 있으며, 내년 초 발매허가를 받을 것으로 전망되고 있다.
또한 보령제약은 선진시장인 유럽, 일본 진출도 본격화하고 있다. 지난 해 12월에는 독일 제약사 AET와 계약을 체결해 유럽 생산기지를 확보한 것은 물론 연내 시범 생산에 들어갈 예정이다. 또한 지난 10월에는 유럽의 허가 기관과 카나브 허가를 위한 사전 절차를 진행하며 유럽진출에 대한 보폭을 넓히고 있다. 지난 6월 임상 승인을 받은 일본에서는 2016년 임상 1상에 돌입했다.
한편 지난해 전 세계 의약품 시장 규모는 무려 1200조원으로, 1인당 의약품에 드는 평균 비용은 4600만원에 달하는 것으로 나타났다. 이에 전문가들은 현재 글로벌 제약시장은 성장세가 빨라 향후 자동차나 전자산업을 뛰어넘을 것이라며 경제 발전에 있어 신성장동력이 될 것이라는 분석을 내놓고 있다.
글로벌 의약품 시장 1200조… 신약, 경제 新성장동력 부상
녹십자-헌터라제·보령-카나브…'제약 코리아' 이끈다
- 조안나
입력 2015-11-20 00:34수정 2015-11-20 09:25
공유하기
기사 공유하기
"한미 7조5천억 잭팟 잇자"... 녹십자·동아ST·보령 등 신약 파이프라인 가동
관련기사
조안나







