4월 식약처 승인받은 국산 37호 신약국내 세 번째 P-CAB 계열 위식도역류질환 치료제위궤양 및 NSAID 유도성 소화성 궤양 예방 등 적응증 확장 임상시험 진행
-
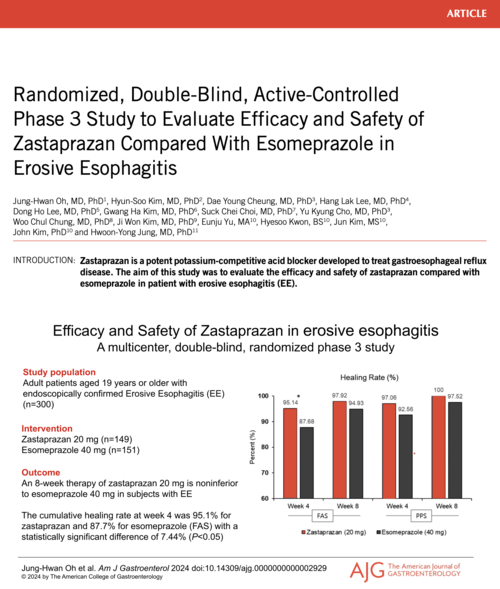
- ▲ 미국 소화기학회지에 실린 자큐보 임상 3상 시험 결과.ⓒ온코닉테라퓨틱스
제일약품의 신약개발 자회사 온코닉테라퓨틱스가 위식도역류질환 치료제 '자큐보정(성분 자스타프라잔)'의 임상 3상 결과가 SCIE급 의학 학술지 '미국 소화기학회지(American Journal of Gastroenterology)'에 게재되었다고 21일 밝혔다.미국 소화기학회지는 논문 피인용지수(임팩트팩터) 10.2로 소화기분야에서 손꼽히는 국제 의학 학술지다.논문 제목은 '미란성 식도염에서 에소메프라졸과 비교한 자스타프라잔의 유효성과 안전성을 평가하기 위한 연구(Randomized, double-blind, active-controlled phase 3 study to evaluate efficacy and safety of zastaprazan compared with esomeprazole in erosive esophagitis)'다.이번 임상 3상 시험은 정훈용 서울아산병원 소화기내과 교수가 국내 주요 병원에서 내시경상 미란성 위식도역류질환 환자 300명을 대상으로 이중눈가림, 무작위 배정을 통해 자스타프라잔 20mg(149명), 대조군 에스오메프라졸 40mg(151명)으로 나누어 최대 8주 동안 약물을 각각 투여하는 방식으로 진행했다.8주 투여 후 자스타프라잔의 치료율은 97.9%로 대조군 94.9% 대비 우수한 효능이 나타났다. 특히, 4주 투여 시 자스타프라잔의 치료율은 95.1%로 대조군 87.7%보다 7.44%p(포인트) 높은 치료율을 보였다.부작용 분석 결과에서 자스타프라잔과 대조군 간 통계적 차이는 없었다. 안전성 측면에서 오랫동안 표준치료제로 사용돼 온 에스오메프라졸과 유사한 수준이라는 의미다.온코닉테라퓨틱스는 현재 자큐보에 대해 위궤양 및 NSAID 유도성 소화성 궤양 예방 등의 적응증을 확대하기 위한 임상시험을 진행 중이다.자큐보는 지난 4월 식품의약품안전처로부터 미란성 위식도역류질환 치료제로 승인받은 국산 '37호' 신약이다. HK이노엔의 케이캡, 대웅제약의 펙수클루에 이어 국내 제약사가 세 번째로 개발한 P-CAB(칼륨 경쟁적 위산 분비 억제제) 계열의 위식도역류질환 치료제다.김존 온코닉테라퓨틱스 대표는 "세계적인 소화기 저널에 임상 3상 시험 논문이 게재돼 전 세계 의료진에게 K-신약인 자스타프라잔의 임상 결과를 공유하게 돼 기쁘다"며 "앞으로 한국 및 해외에서 빠른 상용화를 위해 최선을 다할 것이며 적응증 확대에도 역량을 집중할 것"이라고 말했다.한편, 온코닉테라퓨틱스는 지난해 중국 제약사 리브존파마슈티컬그룹에 자스타프라잔의 중화권 지역 개발 및 상업화 권리를 1억2750만달러(1600억원) 규모로 기술수출했다.







