광유전학 기법으로 미토콘드리아 외막 파괴하는 단백질을 정밀 제어신경세포가 과하게 사멸해 생기는 퇴행성 질환 치료에 새 지평 열어생화학·분자생물학 분야 국제학술지 '익스페리멘털 앤 몰레큘러 메디신'에 게재
-

- ▲ 고려대 이다인 박사(제1저자·왼쪽)와 기계공학부 정석 교수(교신저자).ⓒ고려대
고려대학교는 기계공학부·고려대-한국과학기술연구원(KU-KIST) 융합대학원의 정석 교수 연구팀이 빛을 이용해 세포의 죽음을 억제하는 새로운 기술을 개발했다고 7일 밝혔다.이번 연구는 신경세포가 과하게 사멸해 발생하는 알츠하이머병, 파킨슨병 등 퇴행성 질환의 새로운 치료 전략으로 주목받고 있다.연구팀은 세포 사멸을 유도하는 핵심 단백질인 BAX의 작동 방식을 빛으로 제어하는 데 성공했다. 광유전학 기법을 활용해 BAX의 기능을 억제함으로써 불필요한 세포 사멸을 막고 세포 생존을 유지할 수 있다는 것을 실험적으로 입증했다.
연구팀은 파란빛에 반응하는 단백질 CRY2에 BAX 단백질을 결합하고, CRY2와 빛에 의해 결합하는 단백질 CIB1에는 미토콘드리아 외막 단백질인 TOMM20을 더했다. 이런 구조를 통해 빛을 비추는 것만으로 BAX 단백질이 미토콘드리아로 이동하는 과정을 정밀하게 제어하는 시스템을 구현했다. -
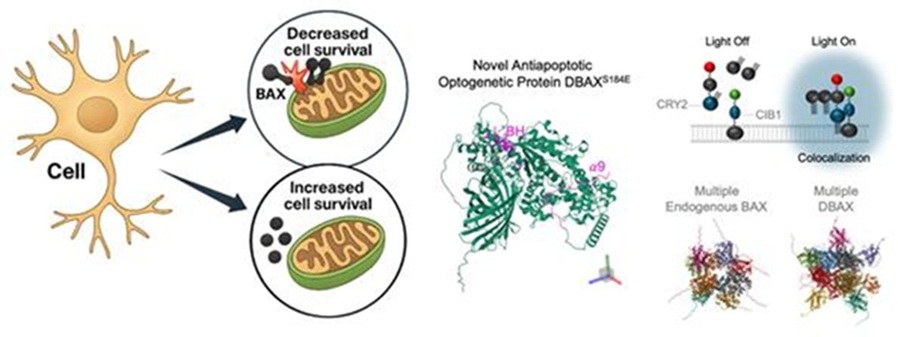
- ▲ 세포 내 미토콘드리아의 활성 유지를 도와 세포 사멸을 저하시키는 신단백질 DBAX(Deterring Bax)의 구조와 여러 분자 물질 결합 시 구멍 형성을 저해하는 모습 요약 이미지.ⓒ고려대
연구팀이 새롭게 설계한 단백질 'DBT(deterring-BAX(DBAX)-TOMM20 복합체)'를 적용한 결과, BAX가 여러 개로 뭉쳐 미토콘드리아 외막에 구멍을 만드는 과정이 효과적으로 억제됐다. 이에 따라 미토콘드리아의 구조가 안정적으로 유지되고 세포 생존율이 크게 향상됐다. 반면 기존 단백질을 적용한 경우엔 세포 사멸이 빠르게 진행돼 뚜렷한 차이를 보였다.이번 연구는 주로 세포 사멸을 촉진하는 방향으로 진행돼 온 암 치료 연구와 달리 세포 사멸을 억제하는 '항 사멸 기술' 개발의 중요성을 부각했다는 점에서 의미가 크다.정석 교수는 "세포 사멸은 생명 유지에 필수적인 과정이지만, 특정 질환에서는 과도하게 진행돼 문제가 된다"며 "이번에 개발한 광유전학적 BAX 조절 기술은 불필요한 세포 사멸을 억제하는 새로운 플랫폼이다. 앞으로 다양한 퇴행성 질환 치료 연구에 폭넓게 활용될 수 있을 것"이라고 말했다.이번 연구 결과는 글로벌 출판사 스프링거 네이처에서 발간하는 의학 전문 학술지 '익스페리멘털 앤 몰레큘러 메디신(Experimental & Molecular Medicine·실험과 분자 의학)'에 지난해 12월 26일 온라인 게재됐다. 고려대 이다인 박사가 제1저자, 정 교수가 교신저자로 각각 참여했다. -

- ▲ ⓒ고려대







