줄기세포 활용해 '미니 뇌' 모델 구현 … 핵심 병리현상 재현 성공특정 빛에 노출되면 형광 빛 내는 조직 대사상태를 이미징 현미경으로 분석세종대 권보미 교수팀·KAIST 유홍기 교수팀과 공동 연구나노과학·기술 분야 국제 저명 학술지 '나노 투데이'에 게재
-

- ▲ 윗줄 왼쪽부터 시계방향으로 고려대 생명공학부 박희호 교수, 세종대 기계항공우주공학부 권보미 교수, KAIST 기계공학과 유홍기 교수(이상 교신저자), KAIST 한정무 박사후연구원, 국민대 손보람 교수, 고려대 강지현 석박사통합과정(이상 제1저자).ⓒ고려대
고려대학교는 생명공학부 박희호 교수 연구팀이 줄기세포를 배양해 실제 장기와 유사한 구조·기능을 재현한 뇌 오가노이드를 이용해 실시간으로 알츠하이머병 진행 과정을 관찰하는 진단 플랫폼을 개발했다고 20일 밝혔다.이번 연구는 알츠하이머병 진단을 위해 특정 형광 물질이나 방사성 물질을 넣지 않고도 조직 자체의 고유한 신호를 분석하는 방식으로 진단이 가능해 주목된다. 별도의 주입 과정이 필요 없고, 생체 상태 그대로 측정하므로 왜곡을 최소화할 수 있으며 반복 검사가 가능하다는 점이 장점으로 꼽힌다.이번 연구는 세종대 기계항공우주공학부 권보미 교수팀, KAIST 기계공학과 유홍기 교수팀과 공동으로 진행했다.알츠하이머병은 전 세계 5000만 명 이상이 앓는 신경퇴행성 질환이다. 미국의 경우 오는 2050년에는 65세 이상 인구 1300만 명이 알츠하이머병을 앓을 것으로 예상된다. 증상이 나타나기 15~20년 전부터 뇌세포가 손상되기 시작한다. 통증이 심한 뇌척수액 채취·분석 또는 고가의 특수 뇌 촬영(PET 이미징) 등을 통해 진단할 수 있다. 조기 발견이 매우 중요하지만, 환자들이 조기에 검사받기에는 건강·비용 측면에서 부담이 크다.기존에는 세포나 동물실험을 통해 알츠하이머병 신약 개발을 추진해 왔지만, 인간 뇌의 복잡한 신경망과 병리적 특성을 완벽히 재현하는 데 어려움이 많았다. -
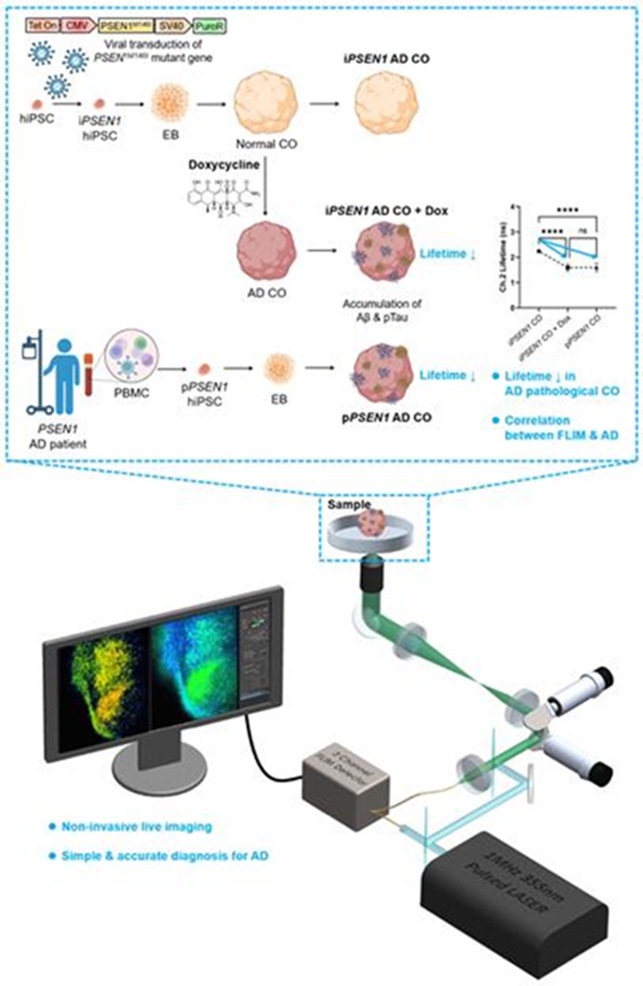
- ▲ hiPSC를 기반으로 구축한 알츠하이머병 뇌 오가노이드 모델과 FLIM 분석 플랫폼의 전체 흐름을 시각화한 그림.ⓒ고려대
연구팀은 환자에게서 채취한 세포에 유전자 변형을 가한 ‘인간 유도만능줄기세포(hiPSC)’를 활용해 뇌 오가노이드 모델을 구축했다. 이 과정에서 가족성 알츠하이머병의 대표적 원인 유전자인 ‘PSENM146I’의 발현 시점을 정밀하게 제어하는 시스템을 설계해 ‘미니 뇌(뇌 오가노이드)’에서 알츠하이머병의 핵심 병리 현상을 재현하는 데 성공했다.연구팀은 멀티모달 형광시상수 이미징(FLIM) 기술(세포 염색 없이, 특정 파장의 빛에 노출되면 나오는 형광 빛을 측정해 조직의 생화학적 특징을 파악하는 기술)을 결합해 살아있는 뇌 조직의 대사 상태를 실시간으로 분석할 수 있는 3차원 프로파일링 플랫폼도 개발했다. 연구팀은 이런 반응이 염증, 산화 스트레스 증가와 상관관계가 있음을 확인했다. 이를 통해 비파괴적인 방법으로 알츠하이머병을 명확히 구별하고, 병의 진행 양상을 실시간으로 추적할 수 있다.박희호 교수는 “살아있는 인간 뇌 오가노이드에서 알츠하이머병의 대사 변화를 비침습적으로 실시간 추적하는 기술을 구현해 기존 진단 패러다임의 전환점을 마련했다”며 “향후 후천성 알츠하이머병을 모사하는 차세대 오가노이드 모델로 확장해 정밀 의료·치료 전략 개발로 이어가겠다”고 말했다.이번 연구 성과는 나노과학·기술 분야의 국제 저명 학술지 ‘나노 투데이(Nano Today)’에 지난달 11일 온라인 게재됐다. 고려대 강지현 석박사통합과정, 국민대 손보람 교수, KAIST 한정무 박사후연구원이 공동 제1저자, 고려대 생명공학부 박희호 교수, 세종대 기계항공우주공학부 권보미 교수, KAIST 기계공학과 유홍기 교수가 공동 교신저자로 각각 참여했다.이번 연구는 과학기술정보통신부·한국연구재단 기초연구실, 산업통상부 합성생물학 기반 혁신 바이오의약품 인재양성사업, 농림축산식품부 고부가가치식품기술개발사업, 해양수산부 대체해조육 및 수산배양육 기술개발연구사업, ㈜심플플래닛의 지원을 받아 수행됐다. -

- ▲ ⓒ고려대







