자가재생치료 모방 '펩타이드' 플랫폼 개발 … 줄기세포 이동·정착 정밀 제어상처부위로 체내·외부 주입 줄기세포 동시에 끌어당겨 … 안정적·경제적화학공학분야 국제 저명 학술지 '케미컬 엔지니어링 저널'에 게재
-

- ▲ 왼쪽부터 아주대 대학원 분자과학기술학과 이예진 석사과정(제1저자), 최상돈 교수, 김문석 교수(이상 공동 교신저자).ⓒ아주대
아주대학교는 대학원 분자과학기술학과 김문석, 최상돈 교수 연구팀이 몸속 줄기세포의 이동부터 정착, 조직 재생까지 단계적으로 유도할 수 있는 ‘액티브 드레싱(Active Dressing)’ 기반 플랫폼을 개발했다고 27일 밝혔다.이번 기술은 체내 미세 환경에서 줄기세포의 행동을 정밀 제어할 수 있는 새로운 재생 의공학 전략으로서 주목된다.기존의 줄기세포 치료는 몸 밖에서 배양한 세포를 질환 치료에 직접 적용하는 방식을 주로 사용했다. 하지만 외부에서 배양된 줄기세포(외인성)의 질환 치료는 타인의 줄기세포 활용으로 말미암은 환자 거부감, 세포치료 안전성, 환자맞춤형 세포 생산의 어려움, 막대한 비용 발생 등의 문제점이 있었다.몸 안에는 내인성 줄기세포가 존재하며, 질환이 발생하면 화학주성인자(Chemoattractant·세포가 화학물질의 농도 기울기를 따라 이동하도록 유도하는 물질)를 통해 이를 질환 부위로 이동시켜 손상된 조직을 치료하는 자가재생치료 메커니즘이 존재한다. -
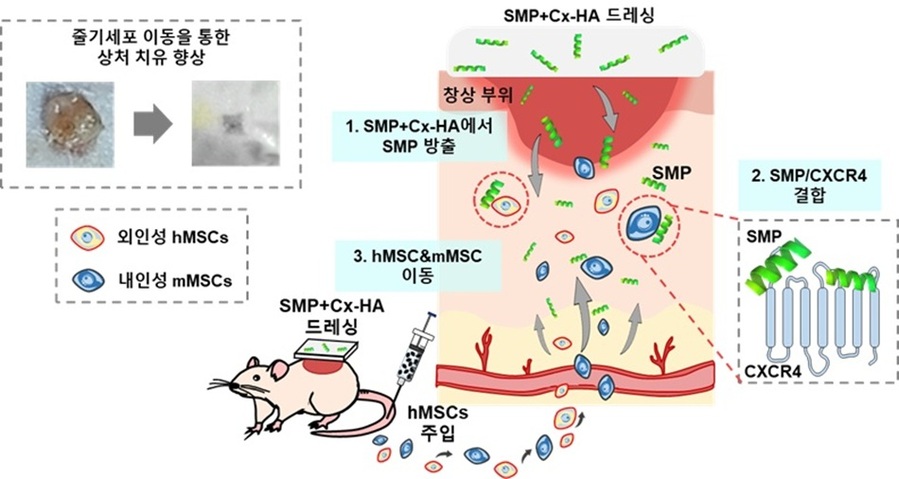
- ▲ 줄기세포의 이동, 정착, 재생까지 제어하는 차세대 액티브 저비용 드레싱의 모식도.ⓒ아주대
연구팀은 외부 배양 줄기세포의 치료 한계를 극복하기 위해 인공지능(AI)을 활용해 화학주성인자 단백질(SDF1) 구조로부터 SDF1 모방 액티브 펩타이드(SMP)를 찾아냈다. 이 펩타이드는 기존 SDF1 단백질 화학주성인자보다 몸 안에서 훨씬 안정적이며 생산 비용도 200분의 1 이하로 경제적이다.연구팀은 SMP 화학주성인자를 통해 몸 안의 내인성 줄기세포를 질환 부위로 지속해서 이동시키는 방법을 고안했다. 생체에 안전한 히알루론산 드레싱(상처에 붙이는 젤·패드 같은 물질)에 줄기세포를 끌어당기는 SMP를 결합했다. 빠르고 정교한 결합을 위해 ‘클릭 화학’ 기술을 적용해 제조했다. 이를 통해 상처 부위에서 SMP 화학주성인자를 천천히 오랜 시간 방출시켜 내인성 줄기세포를 기존 방식보다 10배 이상 많이 이동하도록 유도했다.동물 실험 결과, 이 플랫폼은 외부에서 주입한 줄기세포뿐 아니라 체내에 존재하던 줄기세포까지 동시에 상처 부위로 유도하는 ‘줄기세포 이중 리크루팅(dual recruitment)’ 효과를 보였다. 세포의 초기 유입과 장기적인 조직 재생 과정이 연속적으로 강화돼 혈관 형성과 조직 구조 회복이 크게 향상한 것으로 나타났다.아울러 연구팀은 줄기세포 활성화-이동 및 혈관 형성의 특정 신호 전달 경로 규명을 통해 전체 재생 메커니즘을 규명했다. 이는 개발된 플랫폼이 단순한 드레싱 전달체를 넘어 조직 재생 과정을 체계적으로 설계할 수 있는 기술임을 입증한 것이다. 이번 기술은 향후 당뇨성 궤양이나 만성 창상 등 치료가 어려운 질환에 활용될 수 있다.이번 연구 결과는 화학공학 분야 국제 저명 학술지 ‘케미컬 엔지니어링 저널(Chemical Engineering Journal·화학공학 저널)’ 4월호에 게재됐다. 아주대 분자과학기술학과 이예진 석사과정과 김영훈 석사가 공동 제1저자, 김문석, 최상돈 교수가 공동 교신저자로 각각 참여했다. ㈜메디폴리머도 연구에 참여했다.이번 연구는 한국연구재단의 ‘미래도전연구지원 사업’의 지원을 받아 수행됐다. -

- ▲ 아주대학교 율곡관 전경. 좌측 상단은 최기주 총장.ⓒ아주대







