-
- ▲ (왼쪽 위부터 시계 방향으로) 코젠바이오텍, 씨젠, 수젠텍, 솔젠트의 코로나19 진단키트 ⓒ연합뉴스, 각사
진단 업계조차 외교부가 발표한 미국 식품의약국(FDA)의 사전 승인을 받은 신종 코로나 바이러스(이하 코로나-19) 진단키트를 개발한 국내 업체 3곳이 어딘지 모르는 것으로 확인됐다.
30일 업계와 정부에 따르면 외교부는 지난 28일 보도자료를 통해 "미국 시간으로 27일 국내 코로나19 진단키트 생산업체 3곳의 제품이 FDA로부터 긴급사용승인 절차상 사전승인을 획득했다"고 발표했다.
현재 미국은 코로나-19 분자진단 제품에 대해 미국 식품의약국(FDA)의 긴급사용승인(EUA, Emergency Use Authorization)을 통해 미국 시장에 진출하거나 주 정부가 관리하는 진단검사회사(CLIA Laboratory)의 검증 절차를 통해 시장 진출할 수 있도록 허용하고 있다.
외교부가 언급한 사전승인 획득 단계에 대해서는 업계에서도 의미를 알 수 없다는 얘기가 나온다.
더구나 외교부는 사전승인을 받은 국내 업체 3곳을 밝히지 않았다. 업계 안팎에서는 해당 업체가 어딘지에 대해 관심이 집중되면서 코로나19 진단키트 관련주가 급등하고 있다.
지노믹트리는 이날 오전 9시 10분께 전일 대비 29.88%(4900원) 급등한 2만 1300원으로 상한가를 기록했다. EDGC는 관계사 솔젠트 덕에 이날 오후 2시 10분 기준으로 전일 대비 20.62%(3000원) 급등한 1만 7550원에 거래되고 있다. 같은 시간 씨젠은 전일 대비 2.07%(2400원) 오른 11만 8300원에 거래 중이다.
코젠바이오텍, 씨젠, 솔젠트, 랩지노믹스, 진매트릭스 등이 FDA에 코로나19 진단키트 긴급사용승인(EUA)을 신청했으나 아직 결과를 기다리는 중인 것으로 확인됐다.
FDA 공식 홈페이지의 코로나19 진단키트 EUA 허가 리스트에 국내 업체는 없는 상태다. 심지어 업계에서도 FDA 승인을 받은 국내 업체가 어딘지 파악하지 못하고 있는 상황이다. -
업계에서는 외교부의 발표로 인해 정치적인 부담감이 더해지는 것에 대한 경계심을 드러내기도 했다.
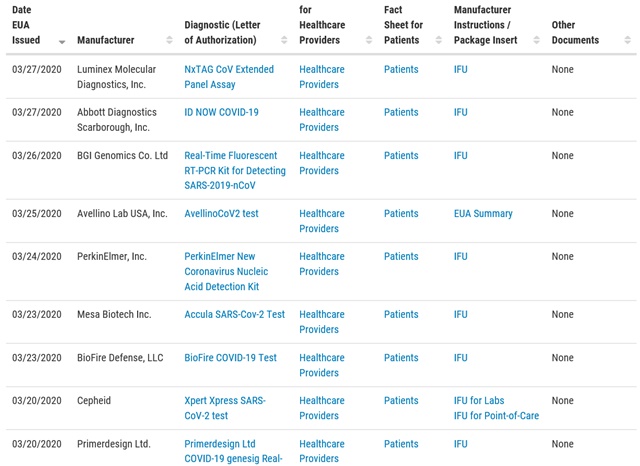
- ▲ 미국 식품의약국(FDA) 공식 홈페이지의 코로나19 진단키트 긴급사용승인(EUA) 허가 리스트에 아직 국내 업체는 없는 상태다. ⓒFDA 공식 홈페이지 캡쳐
한 업계 관계자는 "왜 외교부가 이런 걸 정치 이슈로 끌고 가는지 모르겠다"며 "그러지 않았으면 좋겠다"고 불편한 심기를 내비쳤다.
일각에서는 미국이 주말이라 홈페이지 리스트에 올리는데 시간이 걸리는 중일 수도 있다는 추측도 제기됐다. 30일 오후 2시 기준으로 미국은 월요일이 됐지만 아직 오전 1시이다. 미국의 업무 시간이 시작되려면 오는 31일까지는 허가 리스트 게재를 기다려봐야 한다는 설명이다.
업계 관계자는 "FDA 긴급사용승인을 신청한 상태지만, 아직 확실히 승인 받았다는 레터를 받은 바 없다"며 "FDA 승인을 받으면 당연히 이를 즉각 알릴 것"이라고 강조했다.
업계도 모르는데… 정부만 아는 美 FDA 사전승인 코로나19 진단키트 3곳
- 김새미 기자
입력 2020-03-30 14:21수정 2020-03-30 14:29
공유하기
기사 공유하기
외교부, 28일 보도자료 통해 국내 업체 3곳 美 FDA 사전승인 획득 발표업계 안팎 관심 쏠리면서 관련株 급등… 업계, 정치적 연관 짓기에 부담
관련기사
김새미 기자







